 选择语言
选择语言

多卤素化合物在不同类型反应中的区域选择性一直是困扰大家多年的谜题。如图1所示,2,5-二溴吡啶的芳香亲核取代反应发生在2位[1](亲核取代选择性预测见第1章、第7章、第10章、第19章),钯催化的Buchwald偶联反应也是2位的溴优先反应[2](偶联反应选择性预测见第5章),但是卤素金属交换反应的区域选择性却完全不同,5位溴原子优先反应[3, 4]。
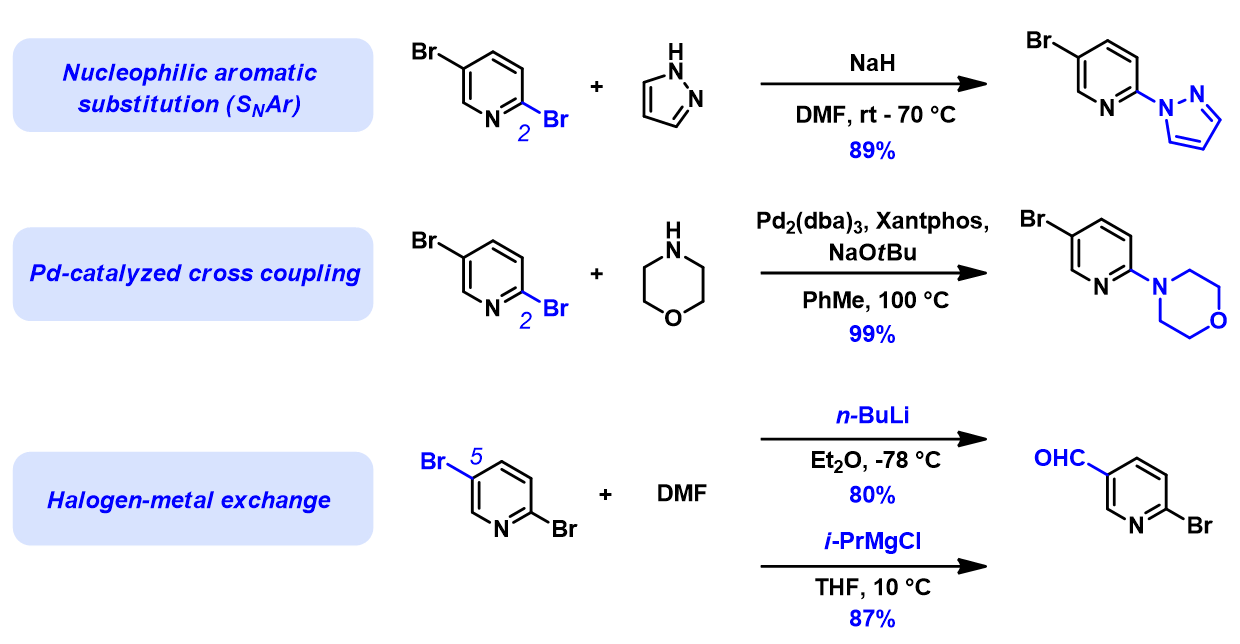
图1. 2,5-二溴吡啶的SNAr、偶联和卤素金属交换反应区域选择性对比
除此之外,还有许多其他的案例,多卤素化合物在亲核取代、偶联和卤素金属交换反应中表现出区域选择性的差异[5, 6]。数十年来,大家一直在寻找这个问题的答案:这种选择性差异的原因是什么呢?
QM作为一项强大的工具,能够帮助我们拨开重重迷雾,看清这些差异背后的真相吗?
首先我们从最简单的溴乙烷化合物开始分析。观察溴乙烷的LUMO lobe分布,C-Br δ键的反方向存在lobe分布,可以接受亲核试剂进攻。β位的C-H键上存在lobe分布,这就解释了为什么溴乙烷在碱性条件下容易发生消除反应。而最引人注目的便是C-Br键上独具特色的“夹心”型 LUMO lobe分布,4个lobe像一串珍珠分布在整个C-Br键上,同时最顶端的lobe体积更大且明显突出于整个分子,可以方便接受金属试剂HOMO的进攻,这就解释了溴乙烷为什么可以与金属Mg等发生卤素金属交换来制备格式试剂。那么,是否可以同样应用“珍珠串”形LUMO lobe分布来解释卤素金属交换反应中的独特选择性呢?
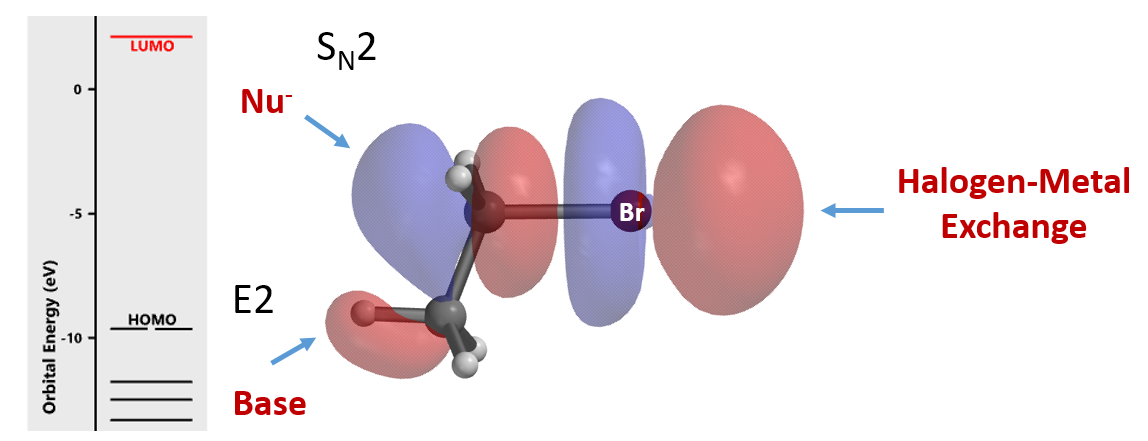
图2. 溴乙烷的LUMO lobe与对应的反应类型[7]
首先,我们尝试用“珍珠串”形LUMO lobe分布来解释2,5-二溴吡啶的溴金属交换反应的选择性。如图3所示,分别计算2,5-二溴吡啶的LUMO、LUMO+1和LUMO+2。LUMO和LUMO+1的C-Br键上没有“珍珠串”形lobe分布。而在LUMO+2上,可以看到5位的C-Br键上有这种独特的lobe分布,lobe体积更大且明显突出于分子Electron Density Map表面,2-位的C-Br键上则没有这种lobe分布。因此,5位的Br可以通过这种独特的lobe与金属试剂更好的相互作用,从而选择性地得到5位C-Br键发生卤素金属交换的产物。
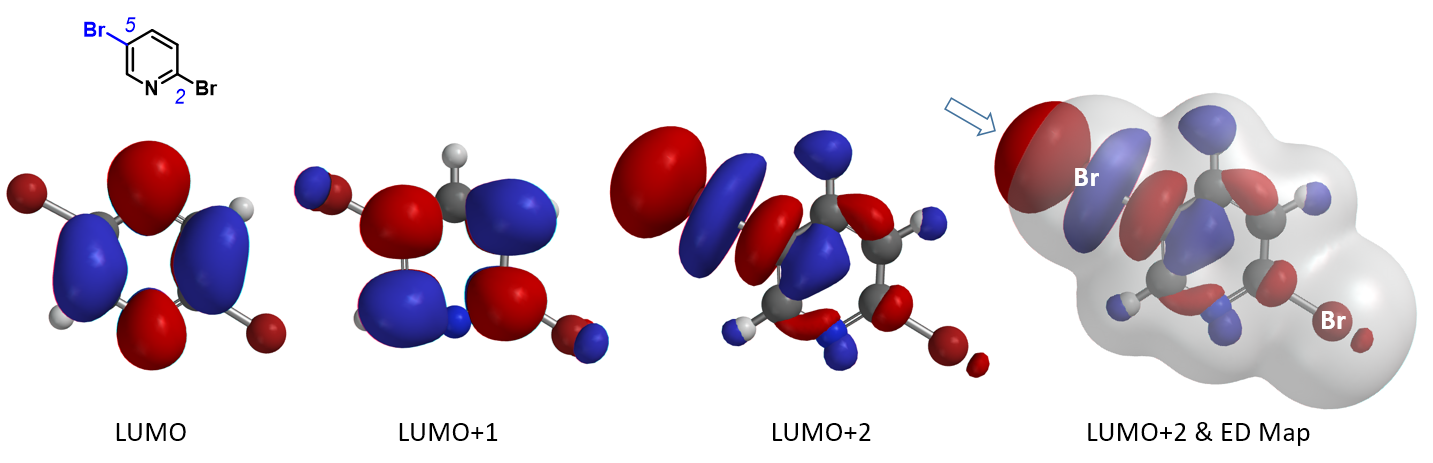
图3. 2,5-二溴吡啶的LUMO、LUMO+1、LUMO+2和LUMO+2与Electron Density Map叠合图[7]
接下来,我们将这个方法应用到更多的案例中(图4)。1,2,4-三溴苯的2-位溴上有体积最大的LUMO+2 lobe分布,与Turbo试剂反应选择性得到2-位取代产物。2,3-二溴噻吩的2-位溴与格式试剂优先反应,2-位溴的LUMO+1 lobe分布明显更大。N-甲基-3,5-二溴吡唑的LUMO显示5位溴的lobe分布明显大于3位溴。N-甲基-5,7-二溴吲哚的LUMO+2 lobe显示7位溴上的lobe体积明显大于5位溴,实验结果也都是lobe分布体积更大的溴原子优先发生卤素金属交换反应。
最后两个案例代表了卤素-金属交换反应的独有特征,就是邻近的甲基基团对反应的位阻影响很小,与之相对应的则是位阻对偶联和SNAr反应影响明显。这种远远超出Electron Density Map的特殊LUMO+n lobe,就可以很好解释卤素金属交换反应对位阻不敏感的原因。

图4. “珍珠串”形LUMO lobe或LUMO+n lobe预测卤素金属交换反应选择性案例[7a-d]
同时,这个方法也可以扩展到直接金属化反应。如图5所示,2,4-二氯-5-氟嘧啶的哪个Cl会更优先在锌粉、醋酸条件下被脱除呢?LUMO+2 lobe分布非常清晰地告诉了我们答案。4位氯的lobe更加明显地突出于分子Electron Density Map表面,因此,它可以优先接受Zn的进攻,形成的锌试剂与醋酸反应。
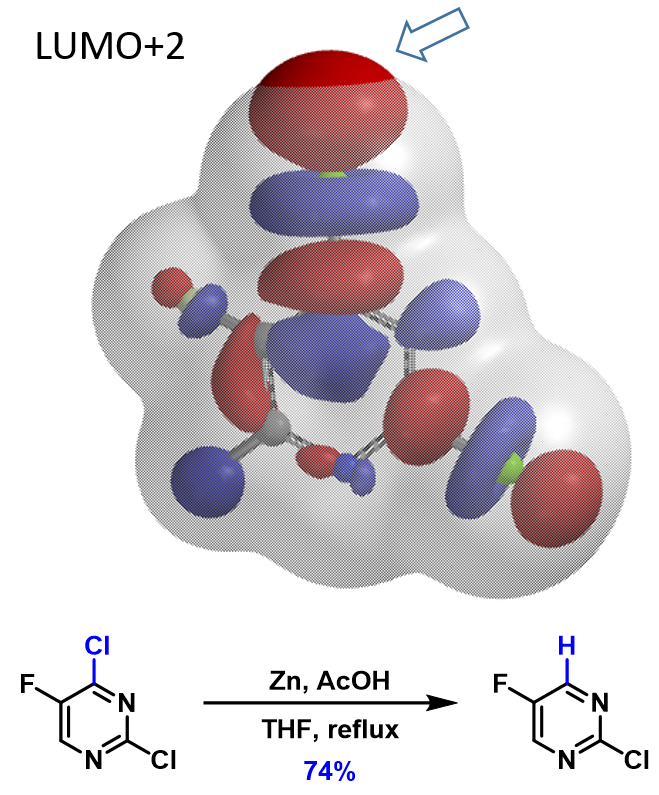
图5. 2,4-二氯-5-氟嘧啶的LUMO+2和Electron Density Map叠合图和脱氯反应[7e]
对于卤素-金属交换反应,利用分布在C-X键上独具特色的4颗“珍珠串”形的LUMO lobe 或LUMO+n lobe,可以让我们准确预测卤素的区域选择性。除了以上6个案例之外,我们还使用该LUMO分析的方法验证了文献报道的100+不同案例。
你可能会有疑问LUMO+2和LUMO+3的轨道能量这么高也可以参与反应吗?当然可以,我们需要考虑的是反应物的HOMO-LUMO能量差(第25章)[8]。n-BuLi和格式试剂的反应活性非常高,对应的HOMO能量也非常高,所以参与反应的LUMO+n轨道能量和HOMO的能量差还在可以发生反应的范围之内。n-BuLi具有比格氏试剂更高的HOMO能量,这也与丁基锂可以在更低温条件下发生卤锂交换的观察一致。
当计算得到的LUMO lobe或 LUMO+n lobe大小接近时,可以进一步比较不同位点反应后形成的芳基金属试剂的相对能量,能量越低,越稳定,在产物中的比例就越高[9]。
虽然真实环境体系中的金属试剂中间体是以碳金属键的形式存在,同时稳定性受溶剂、温度、导向基等各种因素的影响,但是通过简化结构为相应的碳负离子,我们发现计算碳负离子的相对能量也可以很好的预测反应的选择性。
如图6所示,2,3-二溴苯并噻吩的计算结果显示两个Br上的LUMO+1 lobe体积非常接近,实验结果显示以80%的收率选择性得到2位Br发生溴锂交换后的产物[10]。计算两个溴原子反应后形成碳负离子中间体的相对能量,3位溴原子被交换后形成碳负离子的能量比2位形成碳负离子的能量高11.66 kcal/mol,也就是2位溴反应后形成的中间体会更加稳定,因此,选择性得到2位取代的产物。
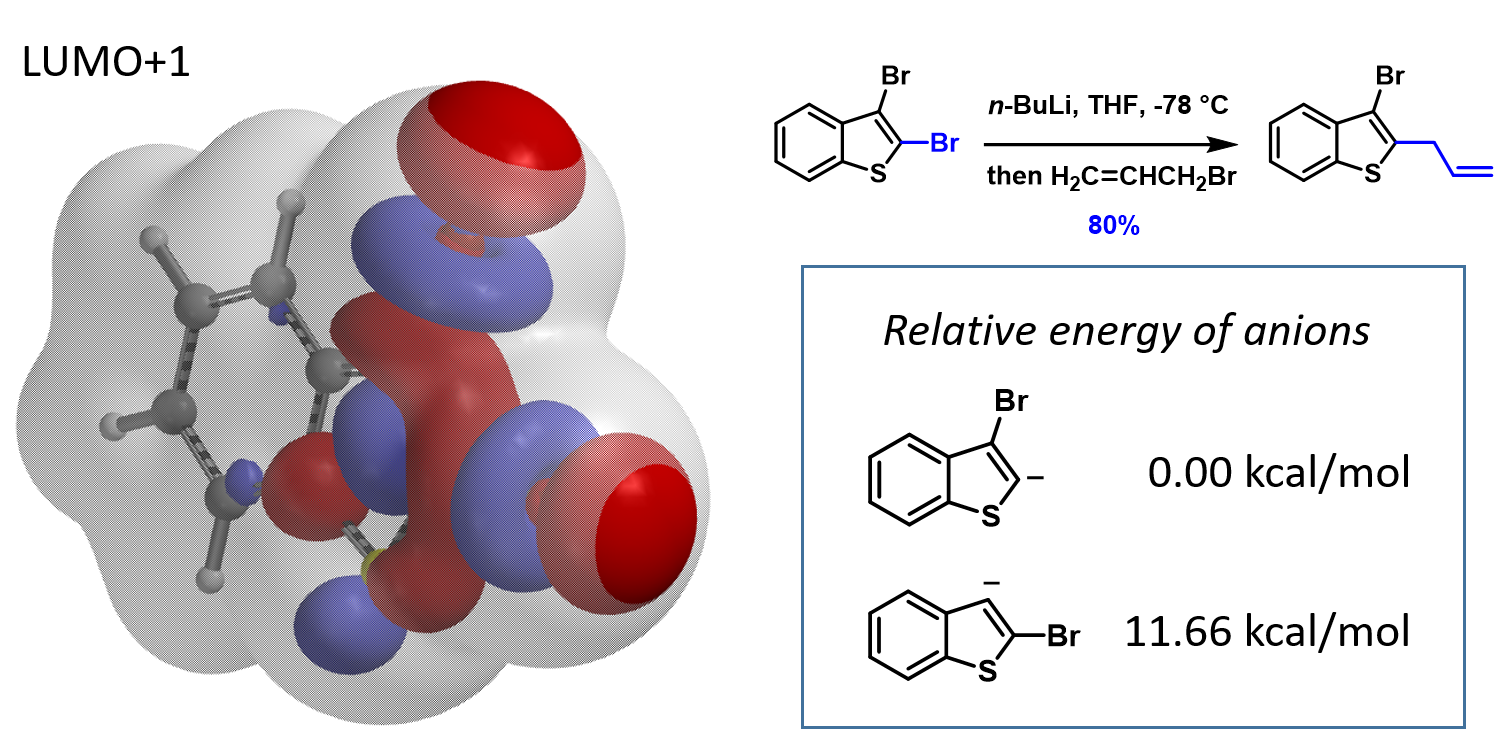
图6. 利用碳负离子相对能量预测2,3-二溴苯并噻吩卤素金属交换反应选择性[10]
总结一下,金属试剂与C-I、C-Br或C-Cl键上独具特色的“珍珠串”形的 LUMO lobe相互作用发生卤素金属交换反应,通过比较卤素原子上这种独特lobe体积的大小就可以让我们准确预测卤素金属反应的区域选择性。这种独特的lobe分布可能是在LUMO上,也可能是在LUMO+1、LUMO+2和LUMO+3上。当LUMO lobe 体积大小接近时,可以进一步计算相应的碳负离子相对能量,碳负离子能量越低,就越稳定,产物的比例越高。氧化加成和SNAr与格氏试剂和锂卤交换的卤素选择性差别,可以通过化学相互作用的量子性质完美解释。前者使用分布在C-X键碳上的LUMO lobe反应,后者使用“珍珠串”形LUMO lobe,它具有非常大的lobe突出于卤化物的Electron Density Map表面,决定了观察到的选择性。
通过将计算LUMO和碳负离子相对能量结合,可以帮助我们准确预测多卤化物发生卤素金属反应的选择性,帮助我们解决了困扰多年的谜题!QM工具在帮助我们解决反应问题的基础上,更可以帮助我们将模糊的反应活性可视化、数据化,为未来构建全息的化学世界奠定基础。
如图7所示,2,5-二溴-4-乙酯噻唑有两种稳定构型,计算结果显示两个构型的LUMO+1 lobe大小正相反,实验结果显示溴-格氏试剂交换反应选择性地发生在C5上[11]。是什么因素在发挥决定性作用呢?
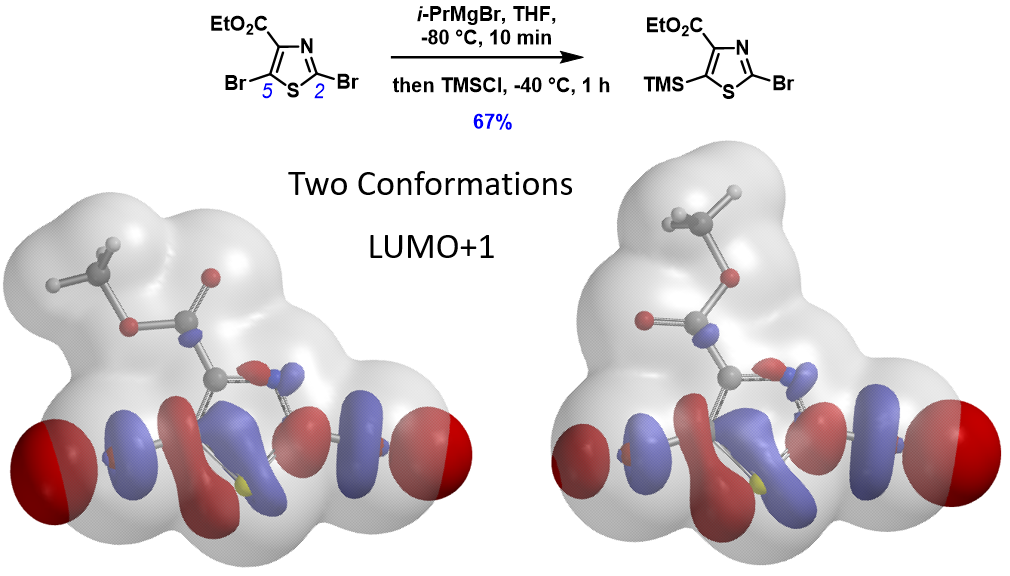
图7. 2,5-二溴-4-乙酯噻唑两种构型的LUMO+1和Electron Density Map叠合图[11]
本文由潘东、刘军、刘文锋、赖光华、卫小文编撰。
参考文献:
[1] C.S. Rani, A.G. Reddy, E. Susithra, K.K. Mak, M.R. Pichika, S. Reddymasu, M.V.B Rao. Med. Chem. Res., 2021, 30, 74.
[2] J.G. Ji, T. Li, W.H. Bunnelle,Org. Lett., 2003, 5, 4611.
[3] P.N.W.Baxter. Chem. Eur. J., 2003, 9, 5011.
[4] L. Peng, J.D. Wen, C.G. Pan, X.W. Pan, Y. Xie, W. He, Q.F. Lin, X.Y. Zhang (Chongqing Sansheng Industrial Co., Ltd., China), CN 112479991 A, 2021.
[5] J.A. Joule & K. Mills, Heterocyclic Chemistry 4th Ed. Malden, MA, USA: Blackwell Publishing Ltd., 2000; pp 26-45.
[6] https://www.scripps.edu/baran/images/grpmtgpdf/Gutekunst_Apr_10.pdf
Divergences in haloselectivity highlighted with 3,6-dibromoindole (pp 2), 2,3,5-tribromo thiophene (pp 3), 2,5-dibromopyridine (pp 6), in palladium catalyzed cross coupling reactions vs halide metal exchange reactions.
[7] LUMO, LUMO+1, LUMO+2和 Electron Density Map在DFT-ωB97X, 6-31G*下计算. (a) A. Krasovskiy, P. Knochel, Angew. Chem. Int. Ed., 2004,43, 3333. (b) C. Christophersen, M. Begtrup, S. Ebdrup, H. Petersen, P. Vedsø. J. Org. Chem., 2003, 68, 9513. (c) Y. Yin, C.J. Chen, R.N. Yu, L. Shu, T.T. Zhang, D.Y. Zhang, Bioorg. Med. Chem., 2019, 27, 1562. (d) P. Anbarasan, H. Neumann, M. Beller, Chem. Eur. J. 2011, 17, 4217. (e) C. De Savi, A. Pape, J.G. Cumming, A. Ting, P.D. Smith, J.N. Burrows, M. Mills, C. Davies, S. Lamont, D. Milne, C. Cook, P. Moore, Y. Sawyer, S. Gerhardt, Bioorganic Med. Chem. Lett., 2011, 21, 1376.
[8] L.G. Zhuo, W. Liao, Z.X. Yu, Asian J. Org. Chem. 2012, 1, 336.
[9] (a) H.J.S. Winkler, H. Winkler,J. Am. Chem. Soc., 1966, 88, 964. (b) H.J.S. Winkler, H. Winkler, J. Am. Chem. Soc.,1966, 88, 969. (c) H.R. Rogers, J. Houk, J. Am. Chem. Soc., 1982, 104, 522. (d) K.B. Kenneth, S. Sklenak, F.B. William, J. Org. Chem., 2000, 65, 2014.
[10] 碳负离子相对能量在nonpolar solvent状态, DFT-ωB97X, 6-31G*下计算. T.P. Sura, D.W.H. MacDowell, J. Org. Chem., 1993, 58, 4360.
[11] M. Abarbi, J. Thibonnet, L. Bérillon, F. Dehmel, M. Rottländer, P. Knochel, J. Org. Chem., 2000, 65, 4618.