 选择语言
选择语言

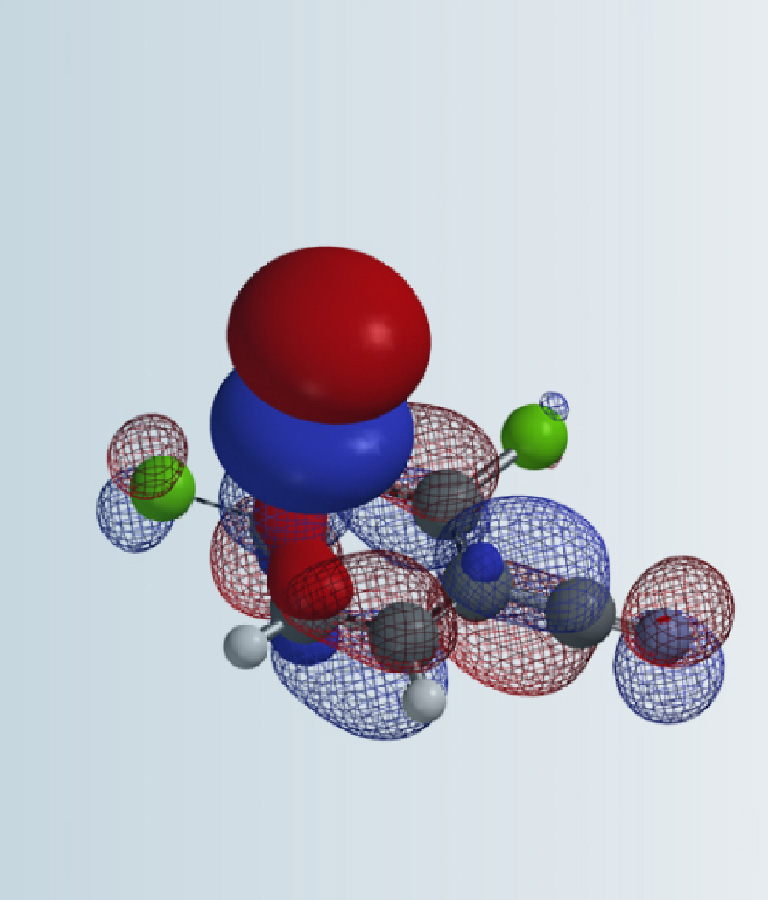
我们在上一章学习了二面角与扭转张力(torsional strain)的相关知识,本章节我们将继续给大家分享“扭转家族”里的另一个知识点——扭转扫描(torsional scan)。扭转扫描计算对于药物化学家来说是一个很有意义的工具,既能帮助分子设计,理解构象与药效的关系,也能评估目标分子合成过程中可能存在的问题。
下面我们从一个实例出发,来展示扭转扫描 QM 计算在药物化学中的应用。
图 1 是两个药物分子的化学平面结构,其中萘啶酰胺 1 与靶标有很强的相互作用,具有较好的生物活性,而喹啉酰胺 2 的生物活性则低很多。
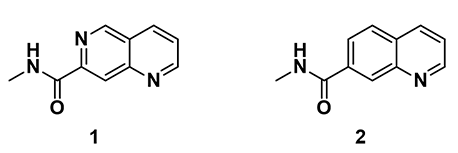
图 1. 萘啶酰胺 1 和喹啉酰胺 2 的化学平面结构
单纯从药物分子的平面结构上看,两者的化学结构非常相似,仅仅是萘啶环上 6 位的 N 原子变成 C 原子后,对酶的生物活性就有天壤之别,我们不禁会问,这是为什么呢?
想要了解这其中的奥秘,就需要我们本章的主角上场了。
借助 QM,我们选取分子中的四个原子,分别对两个药物分子中酰胺平面与芳香平面之间的二面角进行扭转扫描(图 2),以 20° 为步长,计算该二面角从 0° 到 360° 旋转过程中,分子能量的变化。
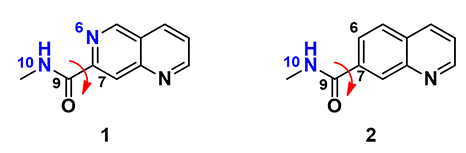
图 2. 萘啶酰胺 1 和喹啉酰胺 2 的扭转扫描平面图
萘啶酰胺 1 的能量变化如图 3 所示,1A 是其低能构象。这一构象中,由于酰胺的N10-H 与萘啶的 N6 之间有氢键作用,酰胺基团与萘啶环呈现出共平面的特征。
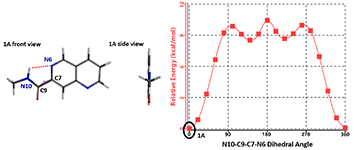
图3:萘啶酰胺 1 的扭转扫描能量图
而喹啉酰胺 2 的分子中(图 4),萘啶环上的 6 位 N 原子变成了 C 原子,导致分子中不仅没有氢键作用,而且酰胺的 N10-H 与 C6-H 之间还会互相排斥。因此,其最低能构象 2A 中,酰胺与喹啉平面之间呈 20° 角(因酰胺有方向性,图 4 能量图中 N10-C9-C7-C6 二面角实际为 200°),且酰胺的羰基氧与喹啉的 C6 原子在同侧。喹啉酰胺 2 若要达到萘啶酰胺 1 的共平面状态,如 2B,则需要额外付出 2 kcal/mol 的能量。
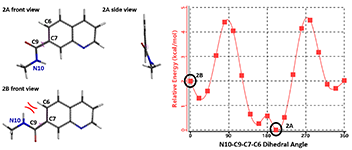
图 4. 喹啉酰胺 2 的扭转扫描能量图
结合萘啶酰胺 1 生物活性更好的事实,我们可以推测,其共平面结构很可能就是与靶点结合的优势构象,且酰胺基团中羰基与胺基的方向也可能有特定的偏好。这就为我们下一步药物分子的设计提供了很重要的信息指导。
扭转扫描可以协助我们分析药物分子的低能构象,及其对生物活性的影响,指导分子设计。另一方面,它还可以帮助有机合成人员分析化合物的旋转异构(rotational isomer)现象,为药物分子的分离和结构鉴定提供线索。
在鉴定吡唑基三氮唑衍生物 3 结构的过程中(图 5),我们通过 1H NMR 谱图可以明显观察到是两个化合物的混合物,因此我们推测是由于吡唑和三氮唑平面之间的 C-N 单键旋转受阻,表现出旋转异构现象,所以产生了混合物。但是当我们利用手性的 SFC 进行分离后,却发现旋转异构体很快重新形成混合物,这又是什么原因呢?
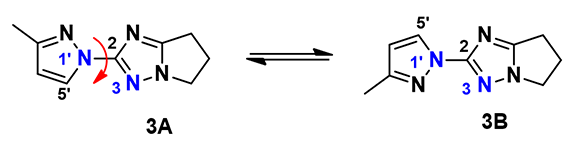
图 5. 吡唑基三氮唑衍生物 3 的旋转异构
我们借助QM工具计算了化合物 3 随 C-N 键旋转时的能量变化图(图6)。
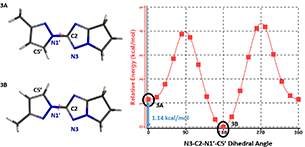
图 6. 吡唑基三氮唑衍生物 3 的扭转扫描能量图
从图中能很直观地观察到两种低能构象 3A 和 3B,两者之间能量差约 1.14 kcal/mol。根据吉布斯自由能变与反应平衡常数的关系 ∆G = −RTlnKeq(其中 Keq =[3B]/[A]),在室温25°C,两种低能构象之间的互变反应达到平衡时,它们的比例为 3A : 3B ≈ 1 : 7。
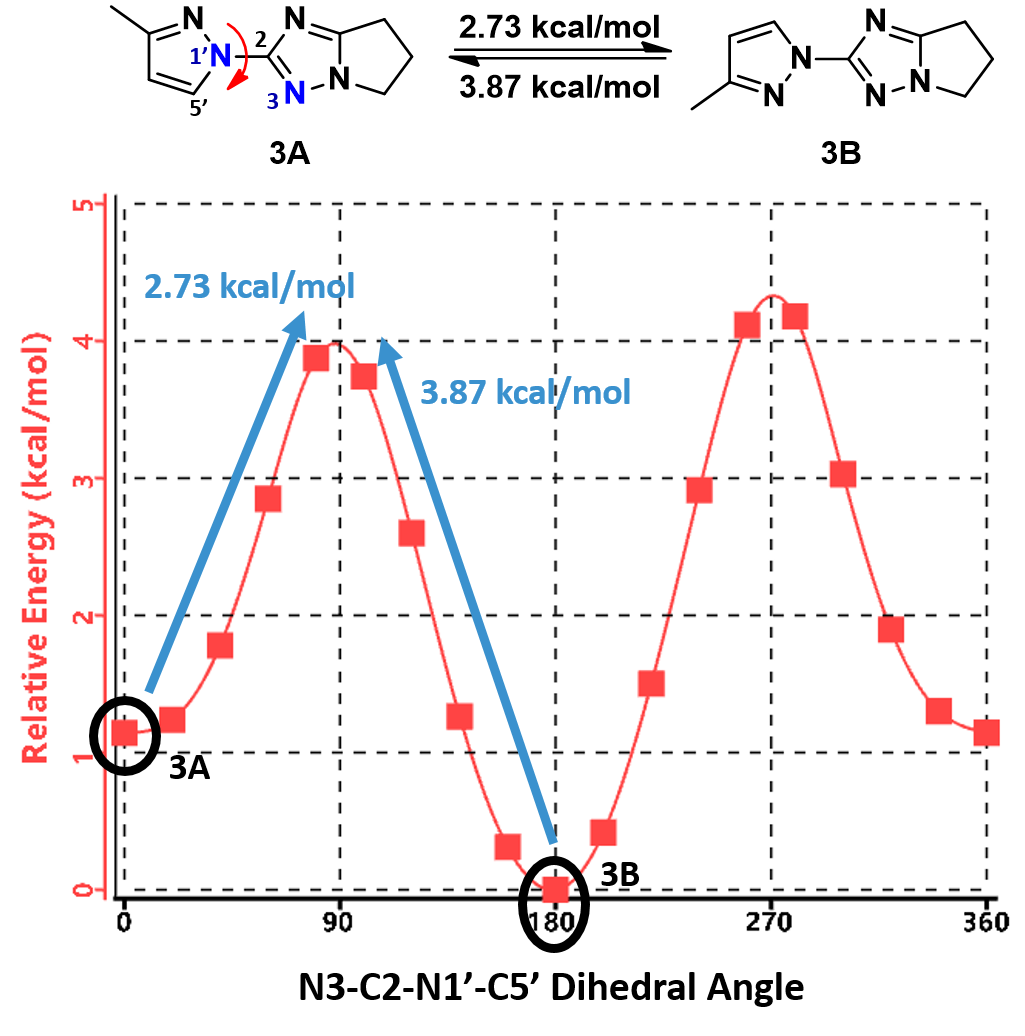
图 7. 吡唑基三氮唑衍生物 3 两种低能构象之间的互变能垒
如图 7 所示,3A 转换成 3B 的能垒约为 2.73 kcal/mol,而 3B 转换成 3A 的能垒则约为 3.87 kcal/mol。由于这两个低能构象之间的互变能垒较高,导致它们的互变速率较慢,足以同时观察到两个旋转异构体的离散信号。但由于互变能垒低于 23 kcal/mol [1](动态能垒),因此我们无法有效分离两个异构体。经分离、浓缩后得到的单一异构体还是会重新回到平衡,转变成混合物(1:7)。
通过本期的两个案例,我们会发现一些看似结构极为相似的药物分子,由于某一原子的变化会使分子的低能构象偏好发生改变,导致生物活性也发生巨变;而当分子中存在旋转异构时,分子低能构象之间互变能垒的高低,也会影响到合成人员的观测与有效分离。这些都说明,化合物分子的立体结构分析,对于药物分子的设计、鉴定、分离有着很深刻的影响。
借助 QM 进行扭转扫描计算,可以帮助我们探究分子的立体特性。希望我们的分享,可以为大家带来启发,助力更多药物研发工作!
本期我们也留了一个相似的案例供大家思考:
图 8 中的吡唑基三氮唑衍生物 4 也具有类似的旋转异构现象。我们在这里提供了该分子低能构象之间的互变能垒图,大家可以尝试计算一下两种低能构象(4A 和 4B)在平衡状态下的比例,以及通过它们的互变能垒来进一步判断,两种低能构象能否在室温下进行有效的分离?
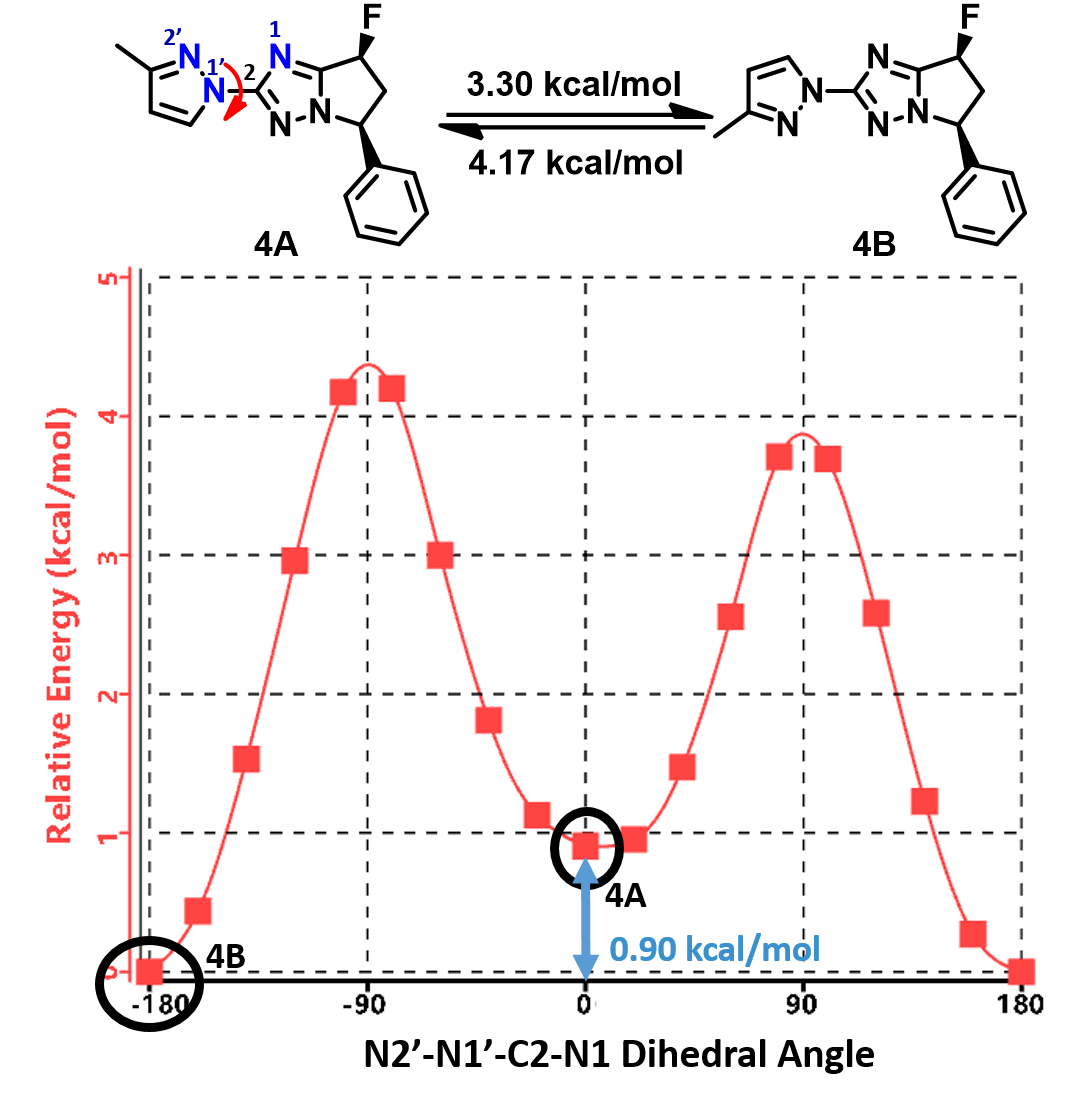
图 8. 吡唑基三氮唑衍生物 4 两种低能构象之间的互变能垒
参考文献:
[1] a) A.M. Belostotskii. Conformational Concept for Synthetic Chemist's Use: Principles and in Lab Exploitation. Hackensack, NJ, USA: World Scientific Publishing, 2015. b)动态能垒(kinetic barrier):室温下,具有较低互变能垒的立体异构体,由于可以迅速互相转化,其在平衡状态下都是以混合物的形式存在。若要有效分离得到单一的同分异构体,它们的动态能垒一般需要至少 23 kcal/mol,此时一对异构体之间互相转化的 t1/2 约为 33 天,两个单一的同分异构体才可能相对稳定的存在。当然,异构体的平衡周期不仅取决于动态能垒,还与环境的物理条件(温度、溶剂)有关。c) S.R. LaPlante, P.J. Edwards, L.D. Fader, A. Jakalian, ChemMedChem 2011, 6, 505.